臨床研究部
臨床研究部の紹介

臨床研究部長
当院の臨床研究部は平成8年9月に設置され、これまで血管疾患とくに動脈硬化症を研究基本テーマとして活動してきました。平成16年4月の独立行政法人化以降、国立病院機構というネットワークを活かした、治験を含む臨床試験、EBM研究および多施設共同研究への参加の占める割合が増してきています。平成20年4月から臨床研究部は研究対象領域を広くして新たにスタートしました。すなわち、従来の血管病センターと連携した動脈硬化症を基本テーマとした循環器分野の研究を継続しつつ、がん総合診療部門と連携したがん領域、当院が専門医療施設として担当する政策医療分野、そして治験を含む臨床試験領域もあらたに加わりました。出来るだけ多くの職員が参加できる研究環境を整えて行く予定です。
大規模臨床試験は治療法の進歩にとって重要です。治験を含む臨床試験への参加は、試験が終了すれば、有用な治療法の開発、無用な薬物の排除、疾患の病態解明のいとぐちを得る等により治療学に貢献したことになり、医師にとっては効果を確認しながら薬物を用いる習慣をつけることにも役立ちます。患者さんも医師も、できるだけ無理なく参加できるように、当院の治験システム改善の取り組みを行いたいと思います。そのほかEBM研究、ネットワーク研究、多施設共同研究への参加や計画立案など、より大きな研究を通して医学へ貢献するための体制づくりも目指したいと思います。
診療と研究は離れたものではありません。患者さんに診療方針を説明するためには、自分自身あるいは診療科の診療内容を印象としてではなく、客観的データとして把握しておくことが必要ですし、データとしてまとめることで日々の診療を振り返ることも出来ます。そして、発表を通して自分の経験を他の人と共有する。普通に行われているこれらの過程をより効率的に行えるようなシステムを作り、各診療科が自分たちの診療指針を持ち改訂を続けることを援助することも研究部の役割であろうと考えています。
臨床研究を行い医学の進歩に貢献する」とは当院の基本方針の一つです。病院職員の研究に対するモーチベーション向上に少しでも役立てるよう、まず臨床研究部のスタッフが、内容はおよばずとも日常診療の中でデータをまとめ、発表してゆく姿勢を持ち続けるよう努力してゆきます。皆様の参加、ご協力をよろしくお願い申し上げます。
院長より
この間、臨床研究部は厳しい医療環境の中にあっても、公的助成研究、院内助成研究、あるいは政策医療ネットワークを基盤とした臨床研究などの研究課題数を着実に積み重ね、輝かしい成果を発表してきた。特に、平成16年4月の独立行政法人化移行はEBM研究や多施設共同研究へ積極的に参加し当院の研究力とともに、その存在を大いに示してきたところである。
さて、これまでの臨床研究部は血管病センターと緊密に連携を保ち運用してきたが、平成20年4月からは研究活動性を高めるために、従来の血管疾患の研究領域に加え、当院の診療特性を活かした研究領域、即ちがん領域や政策医療分野、そして臨床試験領域を新たな研究対象とし、多くの職員が積極的に研究に参画出来る環境を整え再スタートした。
第一線病院における臨床研究部の活動は日々の診療の中から新しい問題点や課題を見出して研究し、その成果は臨床に還元できるものでなくてはならない。国立病院機構の共同研究グループはこれらの社会的ニーズに応じ、研究活動性の高い領域を中心として構築される方針である。当臨床研究部も数多くの研究領域に参画し、質の高い研究に邁進して患者のQOLや臨床成績の向上に貢献出来るよう努力を重ねて頂きたいと願っている。
臨床研究部の更なる飛躍を期待している。
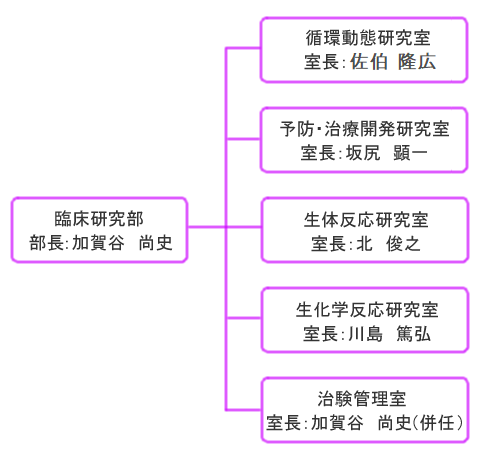
研究室の構成
年度計画
令和8年度 臨床研究部目標
臨床研究部門 加賀谷尚史
1, 臨床研究倫理の周知徹底
➣ 「人を対象とする生命科学・医学系研究に関する倫理指針(令和3年3月23日公布)」を遵守して、正しい手順で臨床研究を実施するよう、院内研究者への周知を徹底する。
➣ 「個人情報の保護に関する法律」の周知を通じて、臨床研究に際しての個人情報保護への意識付けを行う。
➣ 上記のため、臨床研究倫理を学ぶツールとしての”eAPRIN”の受講を推進し、医師に関しては受講率100%を目指す。
2,臨床研究の活性化
➣ 日常臨床からの、臨床疑問を研究につなげることのできるよう、職種を問わず風通しよく意見交換できる土壌を醸成する。
➣ NHO各グループ研究へ、積極的に参加できるよう情報共有を進める。
➣ 金沢大学教授を招請し、特別講演会を定期的に開催することで、臨床研究に取り組む風土を再醸成する。
➣ 各部署/部門・診療科ごとの研究ポイント分析結果を開示し、臨床研究への取り組みを促す。
3.研究成果発信(学会・論文発表)の推進
➣ 研究成果発信に活用できる、統計、翻訳、論文校正の支援を進める。
➣ スタッフの意欲向上のため、発表時の研究費補助制度をより広く周知する。
4、臨床研究ポイントの増加
➣ NHOにおける臨床研究ポイントシステムの周知を進め、ポイントの重みづけについての理解を図る。
➣ 科研費をはじめとした外部資金獲得にむけ、情報の収集と周知を行う。
➣ NHO本部治験への積極的参加のみならず、SMOとの協力もさらに進め、新規治験を獲得する。
➣ 副作用報告、製造市販後調査への積極的対応を進める。
治験管理室について
治験管理室について
各研究室・年度報告
英文論文一覧 各研究室・年度報告助成研究
臨床研究部 「助成研究」の募集について
例年1月31日締め切りで、募集しています。1. 医療全般に関する研究を対象とします。
2. コメディカル分野からの研究も歓迎します。
3. 研究費助成は、1人につき1課題です。15万円以内で申請してください。
4. 来年度までに対外的発表、3年以内に論文誌上掲載出来ることが望まれます。
5. 審査基準に沿って20題前後を採択し、傾斜配分で助成金額を決定します。
6. 採択後に倫理委員会にて研究内容の承認を受ける必要があります。助成研究応募用紙と所定の倫理審査申請書を治験管理室に提出してください。簡易審査の場合は、倫理委員会に出席する必要はありません。あらかじめ審査を受けている場合は不要です。
7. 採択された研究は来年度、院内の臨床研究検討会にて順次発表していただきます。また、所定の用紙に研究結果を記載し、翌年1月31日までに提出してください。
【応募方法】
- 1. 所定の応募用紙(Word形式)に書き込み、E-mail (kawashima.atsuhiro.ka@mail.hosp.go.jp) に添付するか、CD-Rを付けて川島のメールボックス(4F医局)に入れてください。応募用紙は金沢医療センターホームページ(院内、院外)の「臨床研究部」からダウンロードできます。また図書室前パソコンのデスクトップにもあります。
- 締め切り:例年1月31日
- 提出先:臨床研究部 生化学反応研究室長 川島まで
- 応募書類(Word形式)をダウンロードする
- 報告書(Word形式)をダウンロードする
「助成研究」の評価基準
評価項目:
・昨年度の助成研究に対する実績評価
昨年度の助成研究に関する対外的発表(1点)
昨年度までの助成研究に関する論文発表(日本語2点、英語5点)
対外的発表を行っていない(マイナス3点)
研究報告書が未提出である(マイナス2点)
・今年度の研究課題に対する評価
研究に発展性が認められ、臨床的有用性が期待できる(1~5点)
多施設共同研究に貢献する(1点)
助成研究への準備が既になされている(1点)
研究計画が1年間の研究として具体的かつ妥当である(1点)
・過去5年以内の研究発表に対する評価
「助成研究」以外も含めたこれまでの研究発表(1~3点)
公開検討会
1)臨床研究検討会
(毎月第1木曜日、17:30~、第1研修室)
当院臨床研究部主催の研究発表会です。毎回2名の演者が発表し、気軽に討論できる会です。
2)脳心血管疾患カンファランス
(隔月最終木曜日、19:00~、第1研修室)
脳、心大血管、腎、末梢血管など血管をキーワードとして選んだ症例を複数の専門科の視点から眺め、診療方針を討議勉強する検討会です。
倫理委員会
倫理委員会規程はこちら(PDF)
倫理委員会細則はこちら(PDF)
臨床研究の実施に関する手順書はこちら(PDF)
臨床研究における重篤な有害事象等手順書はこちら(PDF)
臨床研究における試料及び情報等の保管手順書はこちら(PDF)
臨床研究利益相反マネージメント規則はこちら(PDF)
臨床研究法における利益相反管理に関する標準業務手順書はこちら(PDF)
臨床研究法上の臨床研究の実施に関する手順書はこちら(PDF)
公正研究遂行のための基本方針
2) 倫理委員会構成員
倫理委員会構成員はこちら
3) 倫理指針
人を対象とする生命科学・医学系研究に関する倫理指針
人を対象とする生命科学・医学系研究に関する倫理指針ガイダンス
4) 倫理委員会 審議課題一覧
令和8年度
*各回をクリックするとPDFファイルが開きます。
| 第1回 | 令和8年4月 開催 | 迅速審査・簡易審査 |
令和7年度 各審査(4月~3月)
*PDFファイルが開きます。
令和6年度 各審査(4月~3月)
*PDFファイルが開きます。
令和5年度 各審査(4月~3月)
*PDFファイルが開きます。
令和4年度 各審査(4月~3月)
*PDFファイルが開きます。
令和3年度 各審査(4月~3月)
*PDFファイルが開きます。
令和2年度 各審査(4月~3月)
*PDFファイルが開きます。
令和元年度 各審査(4月~3月)
*PDFファイルが開きます。
平成30年度 各審査(4月~3月)
*PDFファイルが開きます。
平成29年度
*エクセルファイルが開きます。
【平成29年度】 一括データ
【平成28年度】 一括データ
【平成27年度】 一括データ
【平成26年度】 一括データ
【平成25年度】 一括データ
【平成24年度】 一括データ
【平成23年度】 一括データ
【平成22年度】 一括データ
【平成21年度】 一括データ
【平成20年度】 一括データ
【平成19年度】 一括データ
臨床研究に関するお知らせ
院外研究員の申し込み
希望者は臨床研究部(金沢医療センター;076-262-4161の治験管理室;2585まで)へお問い合わせください。
以下に手続きの流れを箇条書きにまとめます。
- 院外の希望者が院外研究員申請を行い院長が可否を決定します。申請用紙は臨床研究部にあります。期間は2年で延長可能です。
- 共同研究者となる院内スタッフとの調整。検体を用いる場合など、患者さんの同意が必要になる場合がありますが、共同研究者の院内スタッフが主として同意を取ることになると思います。臨床研究部が調整の手伝いをします。
- 研究計画書を作成し、当院の倫理委員会へ提出。倫理委員会申請書類は院内ホームページの管理課セクションからダウンロードできます。
- 倫理委員会の承認後、研究を開始します。
研究部へのご支援のお願い
TEL:076-262-4161 (内線:2432)
FAX:076-222-2758



